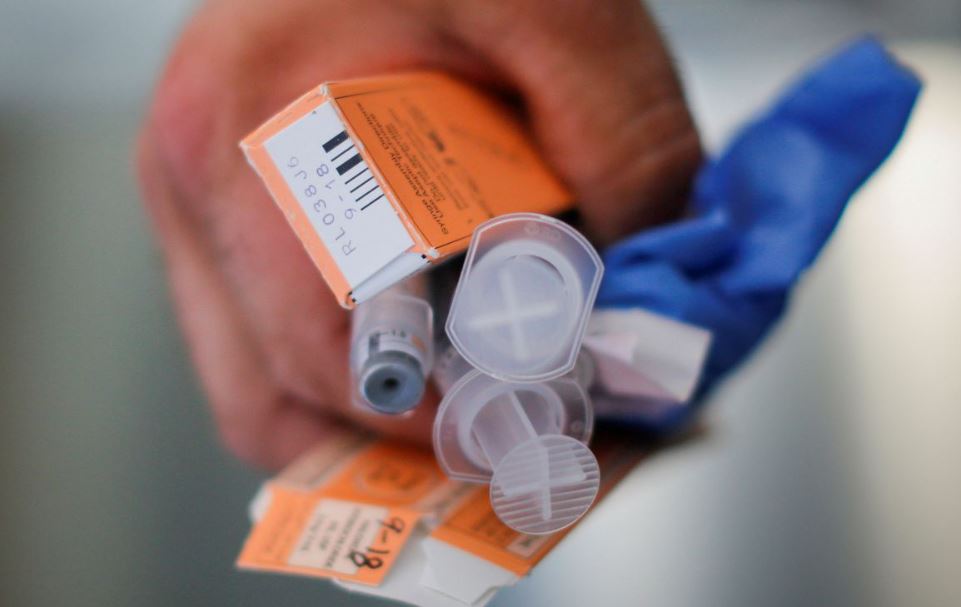
La Administración de Alimentos y Medicamentos (FDA) de Estados Unidos anunció este martes la aprobación del primer aerosol nasal de clorhidrato de nalmefeno para el tratamiento de emergencias por sobredosis de opioides en adultos y pacientes pediátricos de 12 años o más.
“El nalmefeno es un antagonista de los receptores opioides. Si se administra rápidamente puede revertir los efectos de una sobredosis de opioides, incluidas la depresión respiratoria, la sedación y la baja presión arterial”, indicó un comunicado de la FDA.
Lea También: Alerta por la aparición de casos de meningitis tras varias operaciones realizadas en Matamoros
El compuesto aprobado para la farmacéutica Opiant, que lleva el nombre comercial de Opvee, administra 2,7 miligramos de nalmefeno en la cavidad nasal. Está disponible mediante receta y se ha diseñado para su uso en contextos de atención médica y comunitarios, agregó la agencia.
La FDA advirtió que las reacciones adversas al compuesto incluyen molestias nasales, dolores de cabeza, náuseas, mareos, vómitos, ansiedad, fatiga, irritación de la garganta, disminución del apetito, enrojecimiento de la piel y sudor excesivo.